第13回(平成25年度)山崎貞一賞 計測評価分野
マイクロマシン技術のバイオ・ナノ計測への展開
| 受賞者 | ||
|---|---|---|
| 藤田 博之(ふじた ひろゆき) | ||
| 略歴 | ||
| 1980年 | 3月 | 東京大学 工学系研究科 博士課程 修了 |
| 1980年 | 4月 | 東京大学 生産技術研究所 講師 |
| 1981年 | 5月 | 東京大学 生産技術研究所 助教授 |
| 1993年 | 8月 | 東京大学 生産技術研究所 教授 |
| 2000年 | 4月 | 東京大学 生産技術研究所 マイクロナノメカトロニクス国際研究センター長 |
| 現在に至る | ||
| 受賞者 | ||
|---|---|---|
| 野地 博行(のじ ひろゆき) | ||
| 略歴 | ||
| 1997年 | 12月 | 東京工業大学 総合理工学研究科 博士課程 修了 |
| 1998年 | 1月 | 科学技術振興事業団 CREST博士研究員 |
| 2000年 | 10月 | 科学技術振興事業団 さきがけ研究員 |
| 2001年 | 10月 | 東京大学 生産技術研究所 助教授 |
| 2005年 | 4月 | 大阪大学 産業科学研究所 教授 |
| 2010年 | 10月 | 東京大学 工学系研究科 教授 |
| 現在に至る | ||
| 受賞者 | ||
|---|---|---|
| 橋口 原(はしぐち げん) | ||
| 略歴 | ||
| 1988年 | 3月 | 中央大学大学院博士前期課程 修了 |
| 1988年 | 4月 | 新日本製鐵株式会社 入社 |
| 1999年 | 4月 | 香川大学工学部 助教授 |
| 2005年 | 4月 | 香川大学工学部 教授 |
| 2007年 | 9月 | 静岡大学電子工学研究所 教授 |
| 2013年 | 4月 | 静岡大学大学院工学研究科 教授 |
| 現在に至る | ||
授賞理由
現在マイクロマシン(MEMS) の分野は、センサーを中心に広く商品化が進んでいるが、受賞者の藤田博之氏は本分野の黎明期の1980年代から先駆的な研究を行い本分野の発展と実用化に大きく貢献してきた。そして、野地博行氏、橋口原氏と協同して、本技術をバイオナノテクノロジーに貢献する実験ツールに適応し、ナノ物体や分子を直接操作しながら、その形状変化と電気・機械・化学などの諸物性を計測評価する実験系を開発した。
-
特に、
- fL(10-15L)程度の微小容器閉じ込めによる1分子化学力学反応検出
- ナノピンセットによる分子操作、電気特性評価
- 電子顕微鏡中でナノ物体をMEMSで操作し、形状と物性の力学、電気特性を評価した
これらの成果は画期的であり、高く評価できる。
以上の理由により、藤田氏、野地氏、橋口氏の三氏を第13回山崎貞一賞計測評価分野の受賞者とする。
研究開発の背景
シリコンチップの微細加工を利用して、ミクロの機械を作るMEMS(マイクロマシン)技術は、スマートフォンや自動車のセンサとして広く商品化されている。TVゲームで手や体の動きを検出して画面を動かすコントローラや、カメラの手ぶれ防止もMEMSセンサを利用している。一方、科学技術の最前線ではミクロンの千分の一のナノの世界が注目を浴びている。MEMS技術はセンサばかりでなく、ナノ領域での科学実験ツールとして用いられ、ベンゼン環など分子の形を画像化したり、試料表面で原子一つを動かしたりその種類を調べたりできるようになった。
業績内容
本研究では、バイオ・ナノテクノロジー用のMEMS実験ツールを高機能にして、最新の顕微鏡や計測系と組み合わせた実験系を開発し、ナノ物体や生体分子を直接操作しながら、その形の変化と電気・機械・化学等の性質を同時に測った。
- (1)極微小容器内に単一分子を閉じ込めて検出する系:極めて低い濃度のサンプル(例:血中の癌マーカー)を測る原理を図1に示す。微小な球の表面にマーカー分子の抗体を付けておき、サンプル液と混ぜると濃度に比例した確率でマーカー分子が抗体に捕えられる。次にMEMSチップ上に百万個ほど作り込んだ、直径数ミクロンの容器に混合液を閉じ込める。容器の中身は「マーカー付き球」「球のみ」「空」の三種類になる。さらにマーカーを含む容器だけ蛍光で光るバイオ反応を適用すると、光る容器の数が「マーカー付き球」の数を示す。チップ上の球の総数とこれの比から、元のサンプル液が含むマーカーの濃度が計算できる。試験管中で行う従来の手法に比べ、信号対雑音比を百万分倍に改善した高感度検出ができた。
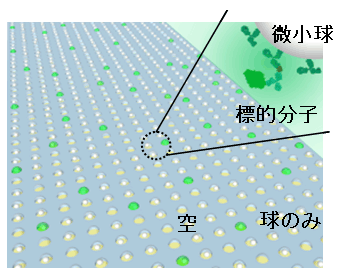
図1 微小容器のアレイで一分子を検出するデバイス
- (2)DNAなどのフィラメント状分子を捕え、機械・電気・化学特性を測定する系:MEMS技術でナノピンセット(図2)を作り、DNA分子やナノ物体を捕獲して電気機械特性を測る研究を行った。DNAの溶液にナノピンセットの先端を浸し、そこに加えた電界の力で分子を水中から引き寄せ、引き延ばした後、ピンセットの腕の両端に橋渡しする形で固定した。捕獲したDNA束を水中に浸してピンセットで力を加え、その硬さを数分子レベルの分解能で測った。水中にDNA切断酵素を加えると分子束が徐々に細く柔かくなっていくが、この時間変化を連続的に測ることに成功した。

図2 MEMS分子ピンセット。左上は針先に捕獲したDNA分子束
- (3)透過電子顕微鏡中のMEMSデバイスで数nmの物体を作り、それに力や電圧を加えた時の形状の変化を見ながら特性を同時に測る系:ナノ物体の引っ張り試験を電子顕微鏡中で行い、細く長く伸びる様子を動画撮影しながら引張応力を測った(図3)。金はほとんど伸びずに切れてしまい、シリコンは元の長さの20倍にも伸びると言う、マクロの世界の常識と正反対の結果が得られた。この他、数ナノメートルの接合では熱伝導が数十倍に増えることが分かった。
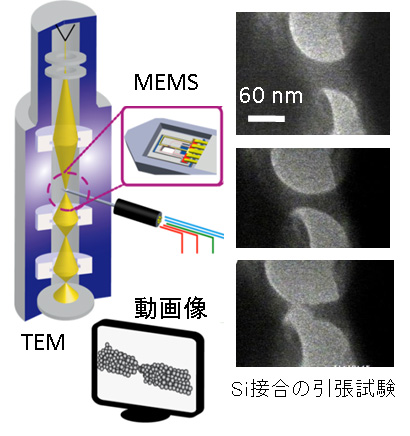
図3 MEMSを透過電子顕微鏡中で動かし、ナノ物体の変化を観測する
本業績の意義
生体分子やナノ物体を調べる時、それに合わせた小さな道具と細部を見る眼が必要だ。本研究の意義は、小さな道具としてマイクロマシンを用い、鋭い眼には光学顕微鏡や電子顕微鏡を使って、極微の世界を解明する点にある。単分子レベルの計測は、臨床検査において癌・神経疾患・感染症等のバイオマーカーを極めて早期から検出したり、尿や唾液など非侵襲で得られる体液を用いて診断したりする新たな市場を創出することが期待される。また、放射線癌治療やある種の抗癌剤では癌細胞のDNAを標的にする。分子ピンセットに捕獲したDNAにX線や抗癌剤を作用させれば、その効果を定量的に測れる。将来は患者のDNAを用いて効果を測り、その人に合った治療法を選択できるかもしれない。最後に電子機器の省電力化や機械の摩擦低減や熱効率向上に、ナノ領域で特異的に現れる特性を利用する考えがある。電子顕微鏡の中でMEMSのツールを使い、このような特性の発見と発現機構を解明することが期待される。
